Carotenoides: os antioxidantes que podem ser produzidos por microalgas
- Priscila Costa Carvalho de Jesus
- Apr 5, 2021
- 7 min read
Este artigo fala um pouco sobre esta importante classe de compostos bioativos.
Fonte: acervo da autora.
Introdução aos carotenoides
Carotenoides são os pigmentos mais amplamente distribuídos na natureza. Eles são uma classe de mais de 700 pigmentos que variam da cor amarela à vermelha.
Os compostos bioativos são geralmente descritos como moléculas que atuam no corpo e podem promover uma boa saúde. Eles são constituintes "extranutricionais" que normalmente ocorrem naturalmente em pequenas quantidades em produtos vegetais e alimentos ricos em lipídeos. A importância dos carotenoides para a saúde humana deriva de seu potencial para reduzir o estresse oxidativo associado a diversos distúrbios, incluindo vários tipos de câncer, doenças neurológicas e cardiovasculares. Os carotenoides (especialmente α-caroteno, β-caroteno e β-criptoxantina) também são importantes precursores da vitamina A, que é essencial para o crescimento e desenvolvimento normais da função do sistema imunológico e da visão (DE CARVALHO; CARAMUJO, 2017).
Aproximadamente 1.117 carotenoides naturais de 683 fontes (entre plantas, algas, cianobactérias, bactérias, leveduras e fungos filamentosos) foram descritos (MUSSAGY et al., 2019). Em organismos fotossintetizantes, estas moléculas atuam na célula na coleta de energia luminosa e sua transferência para clorofila na fotossíntese, bem como fotoprotetores para o aparato fotossintético dissipando a energia excessiva usada na fotossíntese e inibindo a formação de espécies reativas de oxigênio (EROs) (DE CARVALHO; CARAMUJO, 2017). Diversas microalgas contêm essa importante classe de compostos bioativos. Alguns dos carotenoides encontrados em microalgas reportados são: neoxantina, violaxantina, luteína, zeaxantina, ß-caroteno, anteraxantina, astaxantina e cantaxantina (BOROWITZKA, 2013).
Dentre os carotenoides, β-caroteno foi primeiramente produzido por Dunaliella salina, já que esta cresce em altas concentrações salinas, reduzindo o risco de contaminação, além de possuir o maior teor de β-caroteno do que qualquer outro organismo. Outro tipo de carotenoide, produzido pela alga verde Haematococcus pluvialis proveniente de água doce, é a astaxantina, principalmente para o uso como aditivo alimentar para pigmentação da carne nos cultivos de salmão e truta (BOROWITZKA, 2013).
Em relação a diferentes espécies de microalgas, a microalga Chlorella protothecoides apresentou produtividade de luteína na faixa de 4,6 a 5,4 mg/g (massa seca). Outras microalgas que também apresentaram altos níveis de luteína foram Dunaliella salina (6,6 mg/ g), Scenedesmus almeriensis (5,3 mg/g), a microalga vermelha Galdieria sulphuraria (0,4 mg/g), e as microalgas Chlamydomonas planctogloea, Desmodesmus protuberans e Desmodesmus denticulatus, com teor de luteína na biomassa de 7,4, 10,5 e 8,5 mg/g, respectivamente. Sabendo que a atual fonte comercial de luteína são as flores de calêndula, que possuem um teor de luteína de 0,04 a 0,30 mg/g, essas microalgas tem o potencial de produzir cerca de 35 a 250 vezes mais luteína (CEZARE-GOMES et al., 2019).
Em relação a outros microrganismos, diversos trabalhos reportaram a produção de carotenoides intracelulares em diferentes fontes microbianas, além de microalgas, particularmente leveduras e bactérias (MUSSAGY et al., 2019). Dentre as leveduras, Rhodotorula toruloides é considerada uma das mais promissoras para aplicações industriais, por ser fonte de carotenoides, lipídeos e enzimas de alto valor, com produção carotenoides totais de 44,0 ± 2.4 mg/L sob estresse oxidativo (PINHEIRO et al., 2019). Em diversas bactérias isoladas da Antártica, os conteúdos de carotenoides totais variaram de 0,33 a 0,73 mg/g de massa seca (VILA et al., 2019).
A química dos carotenoides
Os carotenoides são moléculas com aproximadamente de 40 a 50 carbonos, altamente insaturadas, e compostas tanto inteiramente de carbono e hidrogênio (carotenos) ou de carbono, hidrogênio e oxigênio (xantofilas).
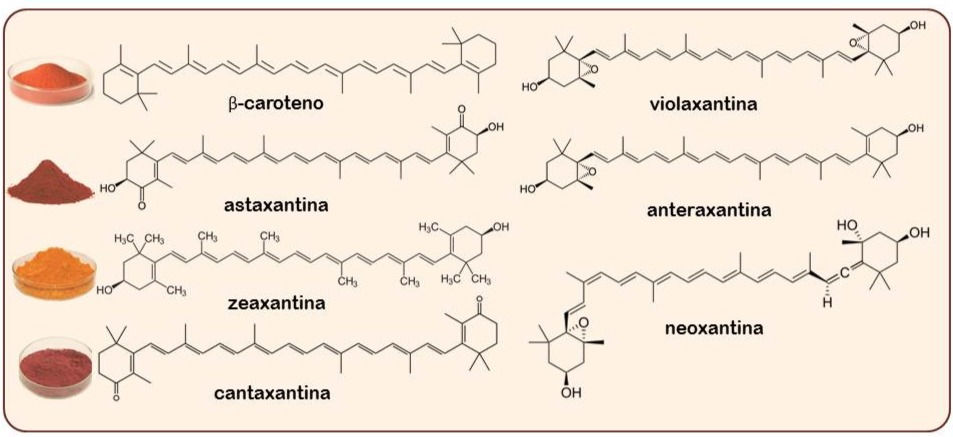
Fonte: acervo da autora.
Em geral, carotenos são mais solúveis em éter de petróleo e hexano, enquanto xantofilas são mais solúveis em metanol e etanol (BRITTON, 1985).
Carotenoides são moléculas altamente conjugadas, o que os tornam suscetíveis à degradação por calor, luz, oxigênio, ácidos e íons metálicos (KOPEC et al., 2012). As duplas ligações conjugadas constituem o sistema cromóforo que confere aos carotenoides a sua cor atrativa e fornece o espectro de absorção na região do visível, que serve como base para a sua identificação e quantificação. A cor permite monitorar qualitativamente as diferentes etapas na análise de carotenoides. Em geral, perda ou mudança de cor durante a análise pode indicar degradação ou modificação estrutural.
Os principais carotenoides comuns podem ser identificados de forma conclusiva pelo uso criterioso e combinado de dados cromatográficos, espectros de absorção na região do UV-Vis e reações químicas específicas para confirmar o tipo, localização e número de grupos funcionais. A espectrometria de massas (MS) e a espectroscopia de ressonância magnética nuclear (RMN) são, no entanto, indispensáveis na elucidação de estruturas desconhecidas ou inconclusivas de carotenoides (BRITTON, 2004).
A maioria dos carotenoides absorve em três comprimentos de onda, resultando num espectro de absorção com três picos seguidos na região do visível. Quanto maior o número de ligações duplas conjugadas, maiores os valores de λmax (PAVIA et al., 2016). Esse é o chamado deslocamento batocrômico, e ocorre porque na presença de ligações duplas conjugadas, os níveis de energia eletrônicos de um cromóforo ficam mais próximos. Consequentemente, a energia necessária para produzir uma transição de um nível de energia eletrônico ocupado para um nível desocupado diminui, e o comprimento de onda da luz absorvida fica maior (PAVIA et al., 2016). Assim, o licopeno, o mais insaturado carotenoide acíclico, com 11 duplas ligações conjugadas, é vermelho e absorve em comprimentos de onda longos (λmax em 444, 470 e 502 nm).
Em relação aos isômeros cis e trans, a isomerização cis de uma dupla ligação de um cromóforo causa uma pequena perda da cor, efeito hipocrômico, acompanhado pela aparição de um pico cis próximo da região ultravioleta (PAVIA et al., 2016).
Uma análise que pode ajudar na identificação dos carotenoides (utilizando o espectro de absorção no UV-Vis) é o cálculo de III/II (%), ou seja, a razão (multiplicada por 100) entre a altura do pico de comprimento de onda mais longo (III) e o pico de absorção do meio (II), tomando como linha de base o ponto de mínimo entre os dois picos. Esse parâmetro, juntamente com o λmax, fornece indícios da estrutura fina espectral do carotenoide, porém pode variar com o solvente utilizado. Em alguns casos, como o ζ-caroteno, III é maior do que II, então o valor de III/II (%) é um pouco maior do que 100. Outros carotenoides, como a cantaxantina e a equinenona, possuem espectros com um único máximo de absorção, não possuindo estrutura fina espectral definida, e então III/II (%) é 0.
O método mais comumente empregado para analisar carotenoides utiliza HPLC (cromatografia líquida de alta eficiência) combinado com detecção por absorção no UV-Vis (NETO et al., 2016). No entanto, os instrumentos hifenados LC-UV-Vis-MS têm se tornado a principal escolha para a análise de carotenoides (CEZARE-GOMES et al., 2019) por fornecer uma análise mais conclusiva, sendo os instrumentos híbridos (QTOF, IT-TOF), que combinam analisadores de diferentes tipos para realizar espectrometria de massas sequencial (MS/MS), utilizados para diferenciar isômeros estruturais e identificar novos compostos (NETO et al., 2016).
Biossíntese de carotenoides em microalgas
Microalgas têm sido utilizadas para transformar CO2 em uma grande variedade de metabólitos industrialmente interessantes.
A figura abaixo (adaptada de MULDERS et al. (2014)) apresenta um esquema simplificado das vias de biossíntese de pigmentos em microalgas.
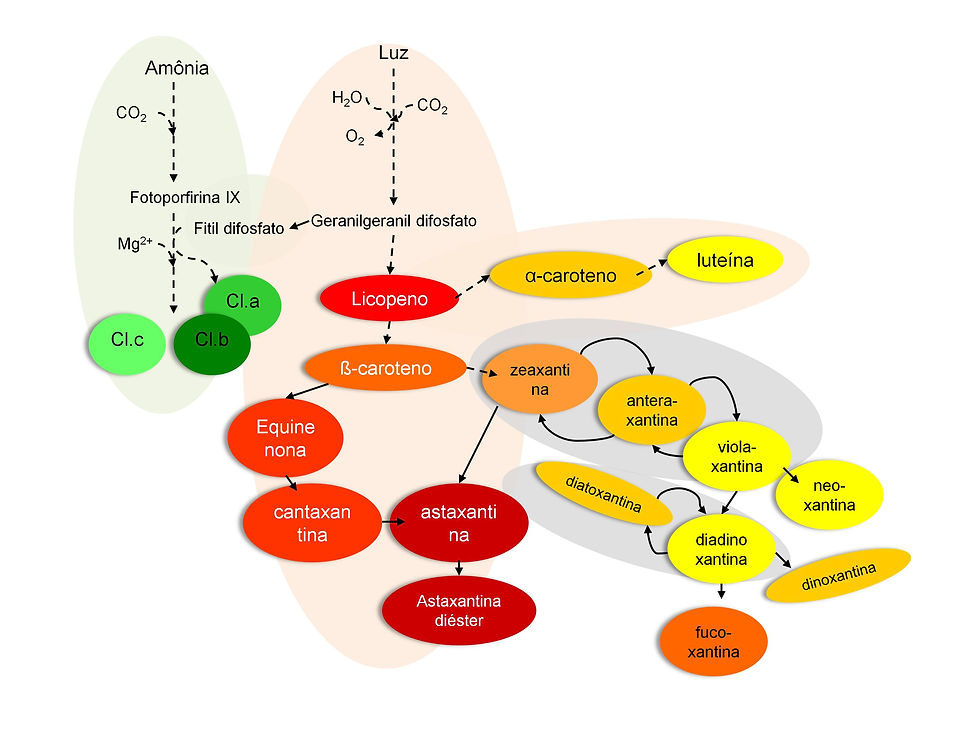
Fonte: adaptada de MULDERS et al. (2014)
A condensação de duas moléculas de geranilgeranil difosfato seguida de uma reação de isomerização e a introdução de 4 ligações duplas formam o carotenoide licopeno. Após a formação do licopeno, as vias sintéticas se separam em duas ramificações. Uma ramificação leva à produção da luteína, a qual em algumas espécies de microalgas, incluindo a Chlamydomonas reinhardti, pode ainda ser convertida a loroxantina. A outra ramificação leva à produção de β-caroteno, o qual também representa um ponto de ramificação. A partir do β-caroteno, uma ramificação leva à geração da astaxantina via duas reações de oxidação e duas de hidroxilação. Este carotenoide hidrofóbico pode ser uma ou duas vezes esterificado com um ácido graxo, levando à formação de mono- ou diéster astaxantina. A outra ramificação do β-caroteno leva à geração de zeaxantina, sendo que alguns autores também propuseram a conversão de zeaxantina a astaxantina na microalga Chlorella zofingiensis. Zeaxantina é parte do ciclo da violaxantina, também referido como o ciclo das xantofilas. Zeaxantina é transformada em anteraxantina e subsequentemente em violaxantina, seguindo duas reações de epoxidação. Violaxantina também pode ser isomerizada, transformando-se em neoxantina (MULDERS et al., 2014).
Carotenoides possuem um papel importante nas células na transferência de energia durante a fotossíntese e na proteção do aparato fotossintético contra danos foto-oxidativos, neutralizando radicais livres e atuando como agentes antioxidantes (PINHEIRO et al., 2019). A produção de antioxidantes por microrganismos fotossintetizantes, em alguns casos, ocorre quando as microalgas estão sujeitas a um estresse, o qual pode ser acompanhado de inibição da divisão celular.
Um dos principais métodos para promover a biossíntese de carotenoides em microalgas é o excesso de luz, sugerindo que o aumento de espécies reativas de oxigênio nessa condição favorece a conversão do precursor de pigmentos em carotenoides em detrimento de clorofila (SUN et al., 2018). Isso pode ser explicado pelo fato de que tanto os carotenoides quanto a clorofila possuem um precursor comum, o geranilgeranil difosato.
Produção comercial de pigmentos
A produção de pigmentos é realizada industrialmente principalmente por síntese química, tendo produzido 1.400 toneladas de carotenoides em 2014, responsáveis por gerar US$ 1,4 bilhão.
Para 2019, eram esperados cerca de US$ 1,8 bilhão, incluindo todas as fontes de carotenoides (sintético e natural). A participação de mercado dos carotenoides de maior sucesso comercial (β-caroteno, luteína e astaxantina) foi de cerca de 60% em 2010. Desse mercado, destaca-se a produção de β-caroteno, representando aproximadamente US$ 270 milhões, dos quais US$ 68 milhões são β-caroteno natural. O preço médio de mercado varia entre US$ 300 e 1.500 kg-1(CEZARE-GOMES et al., 2019).
Astaxantina é o carotenoide de maior valor agregado produzido por microalgas que atingiu maior sucesso comercial. O maior mercado para astaxantina é como fonte de pigmentação em aquicultura, primariamente salmão e truta. Astaxantina era vendida por aproximadamente US$ 2.500 kg-1 (LORENZ; CYSEWSKI, 2000), caindo para cerca de US$ 1.900 kg-1 em 2014 (CEZARE-GOMES et al., 2019). O mercado mundial em 2010 foi cerca de US$ 230 milhões (CEZARE-GOMES et al., 2019). Apesar de 0,95% desse mercado consumir astaxantina produzida sinteticamente, a demanda por produtos naturais tornam os pigmentos sintéticos menos desejáveis e fornece uma oportunidade para a produção de astaxantina natural, principalmente pela microalga Haematococcus pluvialis (LORENZ; CYSEWSKI, 2000). Além disso, astaxantina é um antioxidante 10 vezes mais efetivo do que ß-caroteno, e mais de 100 vezes mais efetivo do que vitamina E (POLYAKOV; MAGYAR; KISPERT, 2013).
Luteína, bem como a zeaxantina, é encontrada em altas concentrações na retina humana. Estudos têm demonstrado que uma dieta suplementada com luteína pode resultar no aumento da quantidade desse pigmento macular e, consequentemente, prevenir algumas doenças degenerativas do olho (KRINSKY; LANDRUM; BONE, 2003). De fato, baixos níveis de luteína e a zeaxantina foram observados em pessoas com catarata (MINHAS et al., 2016). Esses pigmentos foram aprovados pela União Europeia como aditivos e corantes alimentares para a saúde ocular, e o mercado de luteína deve crescer a uma taxa anual de 3,6%. O mercado de zeaxantina ainda é incipiente, porém ambos juntos podem ultrapassar US$ 250 milhões por ano. Atualmente, a principal fonte de luteína são flores de calêndula e não há produção comercial de luteína a partir de microalgas (CEZARE-GOMES et al., 2019).

コメント